ILA er listeført både i Norge og EU (kategori C+D+E), og infeksjon med ILA-virus er listeført av verdens dyrehelseorganisasjon (WOAH). Mistanke om ILA skal straks varsles til Mattilsynet via Altinn. Mattilsynet kunngjør mistanker og stadfestede utbrudd på sin hjemmeside, og melder påvisninger av sykdomsfremkallende ILA-virus til EU-kommisjonen og WOAH. Både mistanke om ILA og stadfestede utbrudd kan påvirke eksporten av laks og regnbueørret.
Smittestoff og smitteveier
Viruset som forårsaker infeksiøs lakseanemi er et akvatisk orthomyxovirus som ligner strukturelt på influensavirus.
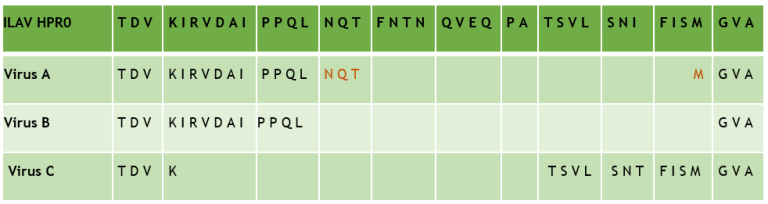
Det skilles mellom ikke-virulent ILA-virus (ILAV HPR0) og virulent ILA-virus (ILAV HPR∆). ILAV HPR∆ utvikler seg fra ILAV HPR0 gjennom en prosess som innebærer forandringer i to overflateproteiner. Delesjon (bortfall) av deler av virusarvestoffet som koder for aminosyrer i den hypervariable regionen (HPR) av virusets hemagglutininesterase, samt forandringer rundt kløyvingssetet i fusjonsproteinet, ser sammen ut til å øke virusets evne til å trenge inn i vertscellen. Dødelighet påvirkes imidlertid ikke bare av virusets egenskaper, men også av forhold som fiskens motstandskraft og ulike miljøfaktorer.
Viruset etablerer seg først i cellelaget (epitelet) som kler fiskens overflate, dvs. slimhinner på gjeller og hud, for så å etablere en infeksjon i cellelaget (endotelet) som kler innsiden av blodkar og hjertet. Til vanlig starter et utbrudd i en merd og sprer seg til nabomerder i løpet av uker og måneder. ILA kan på mange måter karakteriseres som en «ulmebrann», med lav dødelighet, men det er også registrert tilfeller med svært høy dødelighet. Det kan ikke sees bort fra at vertikal overføring av ILA-virus fra stamfisk til avkom i sjeldne tilfeller kan forekomme, men dette betyr trolig lite for spredning av ILA i norske oppdrett.
Epidemiologiske data tyder på at en andel av ILAV HPR0-infeksjoner fører til utvikling av ILAV HPR∆. Utvikling av ILAV HPR∆ fra ILAV HPR0 er den mest sannsynlige forklaringen når isolerte utbrudd oppstår. Det er dokumentert at slike overganger kan finne sted i felt, og at isolerte ILA-utbrudd kan knyttes til utilstrekkelige biosikkerhetsrutiner, som manglende smitteskiller mellom generasjoner og stress. Vi har imidlertid mangelfull kunnskap om hvor stor risiko ILAV HPR0 medfører for utviklingen av ILAV HPR∆, blant annet om andre arter enn laks kan virke som reservoarer, hvor ofte ILAV HPR0 utvikler seg til ILAV HPR∆ og hva som driver denne utviklingen.
Sykdomstegn
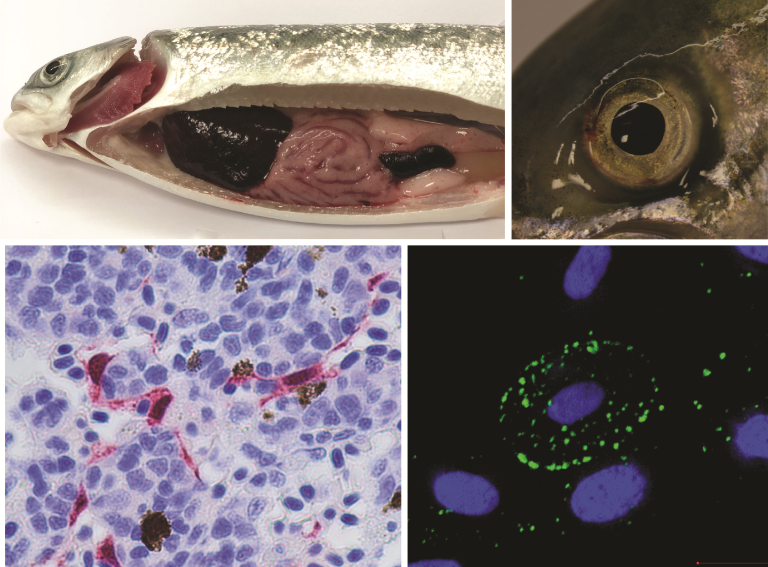
Ved obduksjon finnes som regel tegn på sirkulasjonsproblem, og mer eller mindre alvorlige blødninger i hud og på eller i indre organer. En kan også se mørk lever, svulne nyrer eller milt, eller opphopning av blod i tarmen. Det daglige tapet i merder med syk fisk er ofte forholdsvis lavt, typisk 0,5–1 promille.
ILAV HPR0 er verken knyttet til sykdom eller forandringer i organ (patologi).
Diagnostikk
Personell fra fiskehelsetjenesten eller Mattilsynet obduserer fisk og tar ut relevante prøver i felt. Laboratoriet tar imot en beskrivelse av sykehistorien og synlige forandringer, sammen med prøver av vev fra ulike organer. Både ved mistanke om ILA og overvåkning, vil relevante prøver vanligvis bli undersøkt med real-time RT-PCR først. Dersom det påvises virus, vil den hyperpolymorfe regionen (HPR) bli sekvensert for å avklare om det er ILAV HPR0 eller ILAV HPR∆. Formalinfiksert vev vil bli undersøkt med histopatologiske teknikker for å se etter forandringer som er karakteristiske for ILA, og virus kan påvises ved immunhistokjemi (farging av virus i snitt fra vev) og dyrking i cellekultur. Det er krav om at virus skal påvises med to ulike metoder for å kunne stille en ILA-diagnose.
En større del av arvestoffet til viruset enn kun HPR blir sekvensert fra et utvalg av prøver fra alle lokaliteter hvor det blir påvist virus, så fremt det er tilstrekkelig mengde med virus i prøvene. Slik kan en vurdere graden av slektskap mellom virus som er påvist på ulike lokaliteter, noe som er viktig for smittesporing. I tillegg til å vurdere slektskap mellom virus, er delesjonene i HPR av betydning for å vurdere om smitte mellom to lokaliteter hvor det er påvist identiske eller nært beslektet virus er sannsynlig. Virus med samme delesjon eller kompatible delesjoner er forenlig med smitte mellom lokalitetene, mens virus med ulike, ikke-kompatible delesjoner taler mot smitte mellom lokalitetene selv om virus er nært beslektet og peker i stedet på at virus har et felles opphav, for eksempel i form av ILAV HPR0 som sirkulerer i sjøen eller er til stede på settefiskanlegget.
Veterinærinstituttet er nasjonalt referanselaboratorium for fiskesykdommer og referanselaboratorium for ILA-virusinfeksjon for verdens dyrehelseorganisasjon (WOAH). Med bakgrunn i Veterinærinstituttets forpliktelser som referanselaboratorium, publiseres kvalitetssikrede virussekvenser for segment 5 og segment 6 som påvises i forbindelse med utbrudd, mistanker og overvåking, i en offentlig internasjonal database (GenBank). Sekvensene navnsettes med utgangspunkt i geografisk opprinnelse og år for påvisning, samt journalnummer hos Veterinærinstituttet. For øvrig blir lokalitetsnummer, lokalitetsnavn, dato for prøvetaking og art meldt inn.
Differensialdiagnoser
Flere sykdomstilstander kan forveksles med ILA ved innledende diagnostiske undersøkelser. Dette er spesielt aktuelt i tilfeller der det finnes anemi, forstyrrelser i sirkulasjonssystemet og blødninger. Det er flere kjente tilfeller av ILA der en først har mistenkt CMS, og ILA har også blitt knyttet til problem med vintersår og systemiske infeksjoner med Moritella viscosa.
Overvåkning
I årene 2019 til 2024 utførte Veterinærinstituttet undersøkelser i kartleggingsprogrammet for ILAV HPR0 i norske settefiskanlegg på oppdrag fra Mattilsynet. Nitti fisk på hvert settefiskanlegg ble prøvetatt annet hvert år, og det ble påvist ILAV HPR0 i minst en prøve på omtrent ett av ti anlegg hvert av årene. Den sanne forekomsten er trolig høyere siden infeksjon med ILAV HPR0 er forbigående. På den andre siden er det flere eksempler på at ILAV HPR0 er påvist på samme anlegg ved gjentatte ganger.
Les mer om Kartlegging av ILAV HPR0 i settefiskanlegg.
Alle anlegg som ligger i restriksjonssoner for ILA skal ha månedlige helsebesøk og prøvetaking for å avdekke ILA på et tidligst mulig tidspunkt. Prøvene undersøkes enten hos Veterinærinstituttet eller private laboratorier. Veterinærinstituttet sammenstiller resultatene for Mattilsynet.
Les mer om Overvåking av patogent infeksiøs lakseanemivirus (ILAV HPRdel) i restriksjonssoner i Norge i 2022.
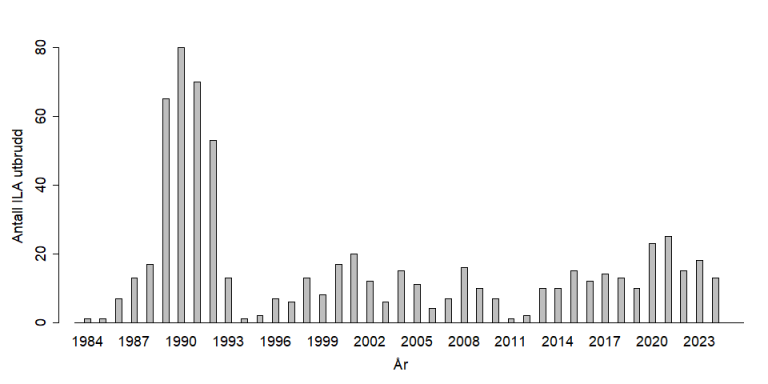
Forekomst
Utbrudd ble første gang påvist i Norge i 1984, og har til nå bare vært kjent hos atlantisk laks i oppdrett. Tallet på ILA-utbrudd per år hadde en topp i 1990 med 80 utbrudd. På slutten av 1980-tallet og starten av 1990-tallet satte Norge i verk en rekke tiltak for å bekjempe sykdommen. Siden 1993 har antall utbrudd variert mellom ett og 25 per år.
I løpet av de siste ti årene er ILA stadfestet i to settefiskanlegg. Begge hadde levert smolt til flere matfiskanlegg hvor det også ble påvist ILA. I begge tilfellene var ILA-viruset på settefiskanlegget identisk eller nært beslektet med viruset som ble påvist på de aktuelle matfiskanleggene. I samme periode er det påvist ILAV HPR0 på omkring ti settefiskanlegg som har levert smolt til ett eller flere matfiskanlegg med ILA-utbrudd. Også her var ILA-virusene som førte til utbruddene identiske eller nært beslektet med ILAV HPR0 på settefiskanlegget som fisken kom fra.
Virulent virus er også påvist hos regnbueørret i forbindelse med utbrudd av ILA hos laks, men det er ikke påvist sykdom hos denne arten. Hvilken rolle infeksjon hos regnbueørret har for smittespredning, er ukjent. Men, det er påvist at infeksjonen hos regnbueørret kan vare i mange måneder.
Utbrudd av ILA er meldt fra de fleste land med kommersiell lakseoppdrett, inkludert Skottland, Færøyane, Chile, Canada og USA.